Europium, symbolen är Eu och atomnumret är 63. Som en typisk medlem av lantanid har europium vanligtvis +3 valens, men syre +2 valens är också vanligt. Det finns färre föreningar av europium med ett valenstillstånd på +2. Jämfört med andra tungmetaller har europium inga signifikanta biologiska effekter och är relativt giftfritt. De flesta tillämpningar av europium använder fosforescenseffekten av europiumföreningar. Europium är ett av de minst förekommande elementen i universum; Det finns bara cirka 5 i universum × 10-8 % av ämnet är europium.
Europium finns i monazit
Upptäckten av Europium
Historien börjar i slutet av 1800-talet: vid den tiden började framstående forskare systematiskt fylla de återstående lediga platserna i Mendelejevs periodiska system genom att analysera det atomära emissionsspektrumet. I dagens perspektiv är detta jobb inte svårt, och en student kan slutföra det; men på den tiden hade forskare bara instrument med låg precision och prover som var svåra att rena. Därför fortsatte alla "kvasi"-upptäckare under hela historien om upptäckten av lantanid att göra falska påståenden och argumentera med varandra.
År 1885 upptäckte Sir William Crookes den första men inte särskilt tydliga signalen för grundämnet 63: han observerade en specifik röd spektrallinje (609 nm) i ett samariumprov. Mellan 1892 och 1893 bekräftade upptäckaren av gallium, samarium och dysprosium, Paul émile LeCoq de Boisbaudran, detta band och upptäckte ytterligare ett grönt band (535 nm).
År 1896 separerade Eugène Anatole Demarçay tålmodigt samariumoxid och bekräftade upptäckten av ett nytt sällsynt jordartsmetall som belägits mellan samarium och gadolinium. Han separerade framgångsrikt detta element år 1901, vilket markerade slutet på upptäcktsresan: ”Jag hoppas kunna döpa detta nya element till europium, med symbolen Eu och atommassan cirka 151.”
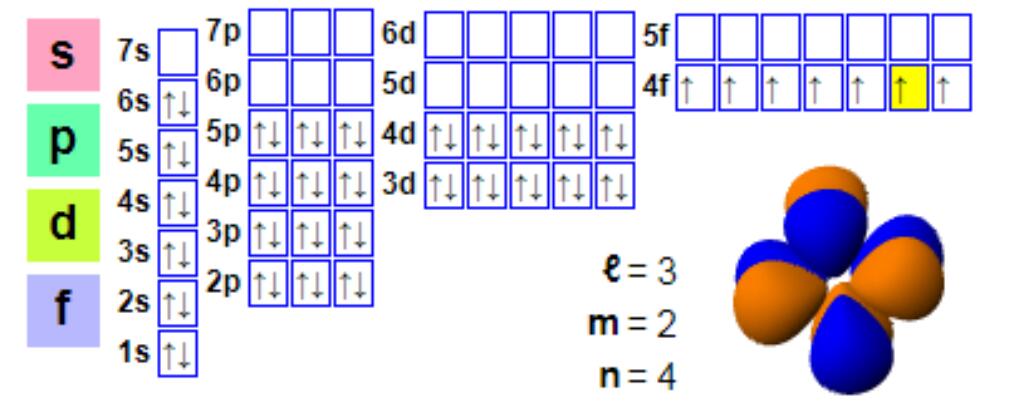
Elektronkonfiguration
Elektronkonfiguration:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f7
Även om europium vanligtvis är trevärt, är det benäget att bilda tvåvärda föreningar. Detta fenomen skiljer sig från bildandet av +3 valensföreningar av de flesta lantanider. Tvåvärt europium har en elektronisk konfiguration på 4f7, eftersom det halvfyllda f-skalet ger mer stabilitet, och europium (II) och barium (II) är likartade. Tvåvärt europium är ett milt reduktionsmedel som oxiderar i luft för att bilda en förening av europium (III). Under anaeroba förhållanden, särskilt uppvärmningsförhållanden, är tvåvärt europium tillräckligt stabilt och tenderar att införlivas i kalcium och andra alkaliska jordartsmineraler. Denna jonbytesprocess är grunden för den "negativa europiumanomalin", det vill säga, jämfört med förekomsten av kondrit har många lantanidmineraler som monazit låg europiumhalt. Jämfört med monazit uppvisar bastnesit ofta färre negativa europiumanomalier, så bastnesit är också den huvudsakliga källan till europium.
Europium är en järngrå metall med en smältpunkt på 822 °C, en kokpunkt på 1597 °C och en densitet på 5,2434 g/cm³. Det är det minst täta, mjukaste och mest flyktiga grundämnet bland sällsynta jordartsmetaller. Europium är den mest aktiva metallen bland sällsynta jordartsmetaller: vid rumstemperatur förlorar den omedelbart sin metalliska glans i luften och oxideras snabbt till pulver. Den reagerar våldsamt med kallt vatten för att generera vätgas. Europium kan reagera med bor, kol, svavel, fosfor, väte, kväve etc.
Tillämpning av Europium
Europiumsulfat avger röd fluorescens under ultraviolett ljus
Georges Urbain, en ung framstående kemist, ärvde Demarçays spektroskopiinstrument och fann att ett yttrium(III)oxidprov dopat med europium avgav mycket starkt rött ljus år 1906. Detta är början på den långa resan för europiumfosforescerande material – som inte bara används för att avge rött ljus, utan även blått ljus, eftersom emissionsspektrumet för Eu2+ faller inom detta område.
En fosfor bestående av röda Eu3+, gröna Tb3+ och blå Eu2+-emittrar, eller en kombination av dem, kan omvandla ultraviolett ljus till synligt ljus. Dessa material spelar en viktig roll i olika instrument runt om i världen: röntgenförstärkande skärmar, katodstrålerör eller plasmaskärmar, såväl som nyare energibesparande lysrör och lysdioder.
Fluorescenseffekten av trivalent europium kan också sensibiliseras av organiska aromatiska molekyler, och sådana komplex kan appliceras i olika situationer som kräver hög känslighet, såsom anti-förfalskningsbläck och streckkoder.
Sedan 1980-talet har europium spelat en ledande roll inom mycket känslig biofarmaceutisk analys med hjälp av tidsupplöst kallfluorescensmetod. På de flesta sjukhus och medicinska laboratorier har sådan analys blivit rutin. Inom life science-forskning, inklusive biologisk avbildning, finns fluorescerande biologiska sonder gjorda av europium och andra lantanider allestädes närvarande. Lyckligtvis räcker ett kilogram europium för att stödja ungefär en miljard analyser – efter att den kinesiska regeringen nyligen begränsade exporten av sällsynta jordartsmetaller behöver industriländer som drabbats av panik över brist på lagring av sällsynta jordartsmetaller inte oroa sig för liknande hot mot sådana tillämpningar.
Europiumoxid används som stimulerad emissionsfosfor i nya medicinska röntgendiagnossystem. Europiumoxid kan också användas för att tillverka färgade linser och optoelektroniska filter, för magnetiska bubbellagringsenheter och i kontrollmaterial, skärmningsmaterial och strukturmaterial i atomreaktorer. Eftersom dess atomer kan absorbera fler neutroner än något annat element används det ofta som ett material för att absorbera neutroner i atomreaktorer.
I dagens snabbt växande värld kan den nyligen upptäckta användningen av europium få djupgående effekter på jordbruket. Forskare har funnit att plaster dopade med tvåvärt europium och envärt koppar effektivt kan omvandla den ultravioletta delen av solljuset till synligt ljus. Denna process är ganska grön (det är komplementfärgerna till rött). Att använda denna typ av plast för att bygga ett växthus kan göra det möjligt för växter att absorbera mer synligt ljus och öka skördarna med cirka 10 %.
Europium kan också tillämpas på kvantminneschip, som pålitligt kan lagra information i flera dagar åt gången. Dessa kan göra det möjligt att lagra känslig kvantdata i en enhet som liknar en hårddisk och skicka den över hela landet.
Publiceringstid: 27 juni 2023